Soluzioni
Servizi
Area tecnica

Via Enrico Mattei, 3
20037 Paderno Dugnano (MI)

La scelta delle diverse tecnologie che si possono utilizzare per lotta all’inquinamento negli ambienti indoor e la bonifica, sanificazione e manutenzione degli impianti aeraulici è determinata da una serie complessa di fattori legati alle caratteristiche chimiche e fisiche degli inquinanti, alle tipologie e volumetrie degli ambienti da trattare, alla destinazione d’uso e alla presenza di forme di vita vegetali o animali. In questo articolo tecnico vengono confrontate le principali tecnologie attualmente disponibili.
Meccanismo d’azione
Un filtro elettrostatico o elettronico è un sistema di filtraggio che permette la separazione del flusso di gas in ingresso dalle particelle inquinanti. Le particelle possono essere sia solide che liquide. Il sistema, attraverso una differenza di potenziale indotta tra degli elettrodi di emissione e di raccolta, realizza la separazione delle particelle contaminanti dal gas vettore che viene fatto fluire tra gli elettrodi. In uscita si ha quindi un flusso d'aria privo di contaminanti.
Un sistema di filtrazione elettrostatica è costituito principalmente da:
Il trattamento consiste nell’applicare un’elevata differenza di potenziale tra gli elettrodi di emissione e di raccolta, in questo modo si ha la creazione, in prossimità degli elettrodi di emissione, di un forte campo elettrico. Il campo generato provoca la ionizzazione del gas (aria) vettore delle particelle contaminanti, attorno alla superficie dell’elettrodo di emissione. L’effetto che si realizza prende il nome di effetto corona. Il flusso di gas che viene fatto passare tra le piastre di raccolta viene ionizzato, quindi gli ioni tendono a spostarsi dalla zona di corona verso gli elettrodi di raccolta. In questa fase gli ioni prodotti entrano in collisione con le particelle di contaminante in sospensione e cedono loro una carica elettrica (ogni particella può essere caricata dall’azione di più ioni, fino a raggiungere elevati livelli di carica). Le polveri cariche vengono quindi attirate verso gli elettrodi di raccolta dove sono trattenute e successivamente rimosse con il metodo a secco o umido. La rimozione dei depositi può anche essere effettuata durante il funzionamento senza dover sospendere la fase di trattamento, impiegando opportuni accorgimenti.
FILTRO ELETTROSTATICO CON MODULI ESTRUSI COMPONIBILI.
Filtro elettrostatico a celle modulari composto da due sezioni separate e distinte, differenti nella tecnologia costruttiva, ed ognuna con le proprie finalità funzionali.
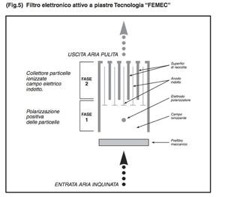 La prima sezione è composta da elettrodi e particolari isolanti (elementi attivi), la seconda è destinata allo sporcamento e quindi alla pulizia e manutenzione (elemento passivo). Le parti attive della prima sezione sono solidali alla struttura portante dove è inserito il filtro stesso. Non essendo esse soggette a manutenzione ordinaria e quindi a manipolazioni, possono essere costruite in modo tale da garantire affidabilità e sicurezza a costi molto contenuti, senza l’impiego di materiali speciali, delicati e costosi (isolatori). La seconda sezione (il collettore) è realizzata in alluminio generalmente estruso, che permette soluzioni dimensionali molto diversificate, le quali consentono di adattarsi alle più svariate esigenze realizzative e d’ingombro. Questa seconda sezione è composta a sua volta in due parti, una passiva collegata a massa finalizzata al collettamento dello sporco e la seconda attiva in quanto sottoposta alla tensione indotta dall’elettrodo polarizzatore. Questa soluzione permette di ottenere campi elettrici sulle superfici contrapposte senza la necessità di un’ulteriore alimentazione elettrica. Inoltre rende ogni zona del collettore indipendente una dall’altra evitando così che un corto circuito accidentale di una sezione possa inficiare il funzionamento dell’intero filtro.
La prima sezione è composta da elettrodi e particolari isolanti (elementi attivi), la seconda è destinata allo sporcamento e quindi alla pulizia e manutenzione (elemento passivo). Le parti attive della prima sezione sono solidali alla struttura portante dove è inserito il filtro stesso. Non essendo esse soggette a manutenzione ordinaria e quindi a manipolazioni, possono essere costruite in modo tale da garantire affidabilità e sicurezza a costi molto contenuti, senza l’impiego di materiali speciali, delicati e costosi (isolatori). La seconda sezione (il collettore) è realizzata in alluminio generalmente estruso, che permette soluzioni dimensionali molto diversificate, le quali consentono di adattarsi alle più svariate esigenze realizzative e d’ingombro. Questa seconda sezione è composta a sua volta in due parti, una passiva collegata a massa finalizzata al collettamento dello sporco e la seconda attiva in quanto sottoposta alla tensione indotta dall’elettrodo polarizzatore. Questa soluzione permette di ottenere campi elettrici sulle superfici contrapposte senza la necessità di un’ulteriore alimentazione elettrica. Inoltre rende ogni zona del collettore indipendente una dall’altra evitando così che un corto circuito accidentale di una sezione possa inficiare il funzionamento dell’intero filtro.
Vantaggi filtro FEMEC:
L’aria mossa dal ventilatore dell’unità di trattamento, prima di entrare nel filtro elettrostatico deve avere:
Il filtro elettrostatico ha un elevato potere germicida dovuto alla sua azione ionizzante con conseguente produzione di piccole quantità di ozono, che contrastano la proliferazione delle sostanze biologiche e contaminanti esistenti sulle superfici delle polveri in transito, ossidandole ed inattivandole.
Sulla base dei dati dimensionali riguardanti i diametri medi dei principali agenti patogeni quali: virus, pollini, acari e funghi, riportati da Sabiana Spa, si può dedurre che tutti i pollini, gli acari ed i funghi elencati vengono captati, inattivati e trattenuti dall’elettrofiltro in rapporto alla sua efficienza. Per quanto riguarda invece i virus, questi, sebbene siano di dimensioni piccolissime, possono essere comunque intercettati, trattenuti e resi inattivi in quanto si presentano sempre uniti e trasportati da particelle di diametro maggiore.
2.3. Produzione di ozono
Nell’articolo “In duct air cleaning devices: Ozone emission rates ad test methodology” sono stati analizzati due precipitatori elettrostatici dal punto di vista della quantità di ozono prodotta. Dai risultati di questa analisi si può notare che entrambi i dispositivi presi in considerazione hanno aumentato la concentrazione di ozono nell’aria in una stanza da 5 a 22 ppb (0.005 – 0.022 ppm). Inoltre, nello stesso studio si è evidenziato che uno dei due dispositivi ha anche registrato elevate emissioni di ozono in presenza di basse temperature.
Con il termine plasma si indica una miscela di gas ionizzati composta da una gran quantità di particelle caricate, come ioni o elettroni, radicali liberi, molecole e anche atomi neutri. La ionizzazione si manifesta quando un elettrone acquisisce sufficiente energia per superare le forze attrattive del nucleo dell’atomo. Quando questo risultato si ottiene con processi che generano un plasma in cui la temperatura degli ioni e degli atomi neutri è sensibilmente minore di quella degli elettroni, si parla di plasma freddo o Non-Thermal Plasma (NTP). Il plasma freddo emette luce con lunghezze d’onda sia nella parte visibile che nella parte ultravioletta dello spettro. Oltre all’emissione di radiazioni UV, un’importante proprietà del plasma a bassa temperatura è la presenza di elettroni ad alta energia, fortemente reattivi, che causano numerosi processi chimici e fisici come l’ossidazione, l’eccitazione di atomi e molecole, la produzione di radicali liberi e di altre particelle reattive. Un plasma si può generare artificialment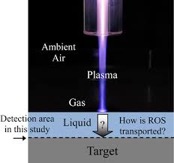 e fornendo ad un gas un’energia sufficientemente alta mediante laser, onde d’urto, arco elettrico, campi elettrici e magnetici, applicando cioè energia a un gas in modo tale da riorganizzare la struttura elettronica delle specie (atomi, molecole) e produrre specie eccitate e ioni. Uno dei più comuni modi per creare artificialmente e mantenere un plasma è l’utilizzo di una scarica elettrica in un gas. Nel caso del plasma freddo, si utilizzano le cosiddette scariche non termiche. I due tipi principali di scariche non-termiche a pressione atmosferica sono la scarica corona e la scarica a barriera di dielettrico.
e fornendo ad un gas un’energia sufficientemente alta mediante laser, onde d’urto, arco elettrico, campi elettrici e magnetici, applicando cioè energia a un gas in modo tale da riorganizzare la struttura elettronica delle specie (atomi, molecole) e produrre specie eccitate e ioni. Uno dei più comuni modi per creare artificialmente e mantenere un plasma è l’utilizzo di una scarica elettrica in un gas. Nel caso del plasma freddo, si utilizzano le cosiddette scariche non termiche. I due tipi principali di scariche non-termiche a pressione atmosferica sono la scarica corona e la scarica a barriera di dielettrico.
Avviene in un gas tra un elettrodo a piccolo raggio di curvatura, chiamato elettrodo attivo, e un elettrodo a larga superficie esterna (elettrodo passivo), tra i quali è applicata una tensione di alcuni kV. In particolare l’elettrodo attivo genera un campo elettrico sufficientemente alto da produrre cariche libere, mentre l’elettrodo esterno anche chiamato elettrodo passivo agisce primariamente come un collettore di cariche. La strumentazione è costituita da un catodo filiforme, dal generatore di corrente e dall’anodo costituito dal componente che viene trattato. Le configurazioni elettrodiche comunemente usate per ottenere l’effetto corona sono la filo-cilindro, la punto-piano e la filo-piano. La configurazione di elettrodi più usata probabilmente è la filocilindro perché assicura una distribuzione abbastanza omogenea della scarica ed è facile da realizzare in un sistema con flusso di gas. Le scariche corona sono suddivise in due categorie: continue e pulsate. Le continue sono prodotte da tensioni in corrente continua o corrente alternata a bassa frequenza. Una corona pulsata è ottenuta applicando un breve impulso di tensione ad un elettrodo. Le due più importanti forme di scarica sono le cosiddette corona a bagliore e corona e “streamer” (scariche a canale o a filamenti). L’instaurarsi di uno di questi due regimi di scarica dipende essenzialmente dalla distanza tra gli elettrodi e dalla evoluzione nel tempo della tensione applicata.
Il gas da cui si genera il plasma viene fatto passare tra due elettrodi metallici, piani e paralleli, tra i quali è presente un materiale dielettrico. La scarica si genera grazie ad una corrente sinusoidale o pulsata che porta alla generazione di micro-archi che hanno luogo grazie all’accumulo di elettroni sullo strato di dielettrico con cui è ricoperto uno degli elettrodi. Il materiale dielettrico impedisce lo sviluppo di correnti elevate. Le configurazioni degli elettrodi più comuni sono le planari con una o due barriere di dielettrico tra gli elettrodi piani. In molte applicazioni tecniche vengono usate anche intercapedini anulari tra elettrodi e dielettrici cilindrici. Le potenzialità di ionizzazione e la densità delle specie cariche generate per il plasma con scarica a corona e il plasma con scarica elettrica a barriera sono diverse:
|
Sorgente |
V(kV) |
Densità (cm^3) |
|
Corona |
10 – 50 |
10^9 – 10^13 |
|
Scarica a barriera di dielettrico |
5 – 25 |
10^12 – 10^15 |
Il trattamento con plasma freddo presenta un importante effetto purificante e sanitizzante. Gli ioni formatisi si uniscono infatti alle particelle in sospensione nell’aria (polveri, aromi, fumo, pollini) caricandole negativamente (o positivamente). Di conseguenza la polvere tenderà a legarsi alle superfici che incontra (le pareti della stanza, per esempio) anziché rimanere sospesa. Per trattare dell’uso della tecnologia NTP per il trattamento dell’aria in locali chiusi bisogna affrontare tre diversi punti:
le descrizioni dei produttori non sono sempre particolarmente chiare nel dare informazioni sulle specie reattive di ossigeno (ROS) che derivano dalla NTP. Bisogna prima stimare se e quali ROS derivano dalle reazioni e poi quali siano le quantità di ROS che queste reazioni generano e introducono nell’ambiente chiuso. Allo stesso tempo, le impurità dell’aria possono essere direttamente attaccate dal NTP e rilasciare ancora altri prodotti.
Poiché i reattori NTP sono universalmente disponibili per la rimozione dei costituenti indesiderati dell’aria, è necessario un generale ripasso delle reazioni tra le impurità dell’aria e i ROS generati.
I moduli NTP svolgono il loro compito senza riserve quando convertono gli inquinanti presenti nell’aria dell’ambiente chiuso con le specie reattive generate il più quantitativamente possibile in sostanze innocue. Universalmente ci si domanda riguardo l’osservanza delle soglie degli effetti collaterali, e non solo in termini di inquinanti dell’aria e dei loro prodotti di degradazione, ma anche rispetto alle sostanze reattive derivanti direttamente dalle reazioni dei sistemi di pulizia dell’aria.
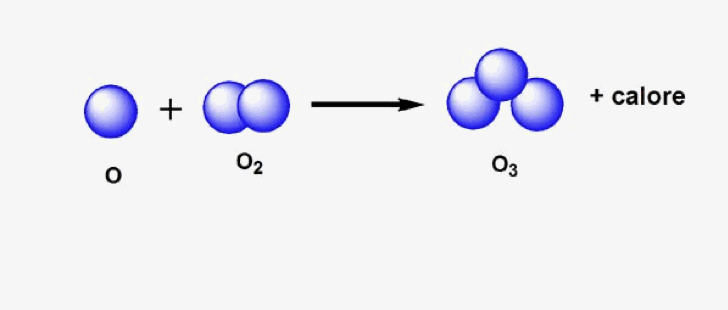
Per generare ozono (O₃), i moduli che sfruttano la tecnologia NTP inizialmente rompono una molecola di ossigeno (O₂) in ossigeno atomico. L’alta energia richiesta per questa reazione (5.16 eV corrispondenti a circa 500 kJ/mol) deriva dalla scarica elettrica. Gli atomi di ossigeno singoli, specie estremamente reattive, possono ora reagire con un’altra molecola di ossigeno (O₂) a formare ozono.
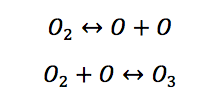
La seconda reazione mostra la reattività dell’ozono e come esso possa rapidamente servire come riserva di ossigeno monoatomico semplicemente ribaltando la reazione.
Nonostante l’energia in ingresso ai moduli che sfruttano la tecnologia NTP sia molto più bassa di quella degli ozonizzatori, l’emergenza ozono è inevitabile come risultato del loro principio lavorativo.
Non è possibile trarre regole generali circa la quantità di ozono prodotta, poiché questo dipende dal singolo dispositivo e dalle sue performance. In base alla relativa lunghezza della vita dell’ozono, il suo rilascio in ranges al di fuori dei limiti è plausibile.
Tuttavia, l’ossigeno monoatomico, a causa della sua reattività, ha una vita estremamente breve e quindi il suo rilascio non è previsto.
|
Specie |
Vita |
| ·O | 0.1 s |
| ·OH | 1 s |
| ·OOH | 1 min |
| O₂ (∆g) | < 64 min |
| O₂⁻ | s / min |
| O₃ | 1 mese |
| H | Estremamente breve |
| N | Estremamente breve |
| NO | 1 giorno |
| NO₂ | Parecchi giorni |
| HNO₃ | Parecchi giorni |
In connessione con la tecnologia NTP, si fa spesso riferimento all’ossigeno singoletto come un reagente. Con questo termine si fa riferimento a una forma di molecola di ossigeno che cambia in differenti stati di reazione assorbendo energia. Sebbene la quantità di energia richiesta per questo (0,98 eV corrispondenti a 94,3 kJ/mol) non sia particolarmente grande, questa forma di eccitazione è legata a speciali condizioni. Le regole della chimica teorica affermano che questa attivazione sia improbabile in assenza di un catalizzatore. In forti campi elettrici come quelli presenti nei moduli con tecnologia NTP, queste speciali condizioni sono di fatto presenti. Tuttavia non ci sono forti evidenze in letteratura di questo e rimane ancora poco chiaro se l’ossigeno singoletto sia realmente generato in misura apprezzabile.
Il radicale ossidrile deriva dalla reazione dell’ossigeno atomico con l’acqua (H₂O) e anche come possibile prodotto di ozono e composti insaturi. È caratterizzato dalla sua reattività relativa con stabilità relativamente elevata e lunghezza della vita di circa un secondo. Il suo rilascio, anche se minimo, dalla camera di reazione di un modulo con tecnologia NTP non può tuttavia essere escluso.
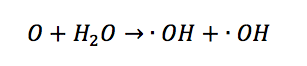
Gli elettroni rilasciati durante la scarica elettrica possono incoraggiare la riduzione della molecola di ossigeno a produrre il radicale anione del superossido (O₂⁻). La presenza di acqua porta alla formazione del radicale idroperossido (). La rottura di una molecola di acqua a formare atomi di idrogeno e radicali ossidrili è un ulteriore fonte di specie reattive. Dalla reazione con ossigeno o ozono, entrambi possono generare il radicale idroperossido (). L’aria consiste per il 78% di azoto che, come la molecola di ossigeno, ha forma di molecola diatomica N₂. la dissociazione della molecola di azoto fornisce azoto monoatomico. Questo, tuttavia, richiede una quantità di energia molto più alta della reazione equivalente della molecola di O₂ e può quindi essere prevista solo in misura molto limitata, se non del tutto, nei moduli con tecnologia NTP.

Le scariche elettriche nei moduli a scarica sono fondamentalmente capaci di iniziare le reazioni dirette delle impurità organiche. A seconda del loro tipo, queste possono convertirsi per assorbimento di elettroni in anioni radicali. Questi li attivano per successive reazioni con le altre sostanze presenti, come ROS o altri componenti dell’aria, oppure si stabilizzano mediante frammentazione. Lo stesso vale per le conversioni dirette con i ROS: è plausibile una moltitudine di differenti prodotti, e nell’eventualità della frammentazione è possibile anche un aumento nella concentrazione di inquinante. La quantità dipende ancora dalle performance e dalle caratteristiche dei moduli NTP e non possono essere stimate senza indagini sui singoli dispositivi.
I moduli NTP promettono un aumento del benessere e un miglioramento della salute mediante la generazione di ioni negativi. Tuttavia, è anche risaputo che le particelle di aerosol contenute nell’aria degli ambienti chiusi formano nuclei di condensazione mediante carica elettrica e questi nuclei precipitano velocemente dopo la loro agglomerazione. Questo porta a una riduzione di concentrazione delle particelle, sebbene un effetto apprezzabile dipenda fortemente dalle performance del dispositivo usato e dalle dimensioni della stanza. Ci sono tuttavia studi che mettono in dubbio un effetto marcato o duraturo di questi.
L’ossigeno monoatomico è uno degli ossidanti più aggressivi. Con il suo aiuto, è possibile convertire completamente gli inquinanti organici dell’aria (VOCs = Volatile Organic Compounds) in composti semplici come il diossido di carbonio e l’acqua, sempre che sia abbastanza disponibile. Eteroatomi come zolfo e azoto, che possono essere contenuti nei VOCs, possono risultare inevitabilmente nella formazione di ossidi di zolfo e azoto.
Allo stesso tempo, la generazione di grandi quantità di ossigeno monoatomico nelle reazioni dell’NTP non è desiderabile a causa delle simili grandi quantità di ozono che si presenterebbero. A causa degli enormi eccessi di ossigeno biatomico in relazione alle possibili impurità dell’aria (21% comparato con < 1 ppm di impurità dell’aria), piccole concentrazioni si combinerebbero principalmente con ossigeno monoatomico a formare ozono. Questo significa che gli inquinanti dell’aria possono essere decomposti da reazioni dirette con ossigeno atomico per produrre prodotti parzialmente ossidati. In conversioni non specifiche, questo può risultare in nuovi composti.
Reazioni di ozono con composti organici sono state frequentemente descritte in letteratura. L’ozono è in parte usato perché è utile per conversioni selettive in forma di ozonolisi. Questo significa che con l’aiuto dell’ozono alcuni specifici gruppi funzionali di molecole organiche possono essere modificati senza attaccare il resto della molecola. Se le reazioni con ozono sono incontrollate (come nei moduli NTP), questi gruppi funzionali sono attaccati in modo preferenziale. Per esempio via ozonizzazione si possono produrre idrocarburi insaturi e diversi gruppi di composti come acidi carbossilici, aldeidi, chetoni e idroperossidi. Idroperossidi del tipo decomposti ulteriormente, rilasciano radicale ROS ossidrile. Con le concentrazioni di ozono nel range da ppm bassi a ppm alti, la conversione quantitativa di inquinanti atmosferici in e non può essere prevista.
Se l’ossigeno singoletto è formato in quantità apprezzabili, sembra poter avere uso limitato solo come purificatore d’aria. Nel NTP ci si possono aspettare prodotti di reazione associati, per esempio composti del perossido, eventualmente seguiti da riarrangiamenti. Ciò contrasta con la rottura completa prevista di un’ampia gamma di sostanze inquinanti.
Dei ROS rimanenti, il radicale ossidrile ( · OH) è il più importante. Esso è fortemente reattivo e attacca gli inquinanti organici dell’aria ad esempio composti insaturi, aromatici e aldeidi. Una vasta gamma di prodotti può quindi essere prevista (radicali alchilici R · , radicali alcossilici RO · , radicali alchilperossilici ROO · ).
Una rottura parziale o completa dei prodotti primari è improbabile a causa delle piccole quantità coinvolte e la quasi completa mancanza di successive reazioni fotochimiche negli ambienti chiusi.
E’ improbabile che i moduli NTP incoraggino la formazione di ossidi di azoto dall’ossigeno atmosferico in quantità apprezzabili. Tuttavia, fino a una media di 100 ppb di monossido di azoto (NO) è possibile in ambienti interni come conseguenza dell’armonizzazione con le concentrazioni dell’aria esterna. In questa misura, si può quindi assumere che si formi diossido di azoto (NO2) da NO e ossigeno monoatomico, ozono o idroperossido ( · OOH).
Ulteriori prodotti successivi sono triossido di azoto (NO3) e pentossido di di ossigeno (N2O5), dai quali con acqua (dall’umidità atmosferica) o con i VOCs si forma acido nitrico.
L’idea di utilizzare l’ossigeno per la rimozione delle impurità dell’aria in ambienti chiusi a beneficio della salute e dell’ambiente sembra a prima vista utile e promettente. Tuttavia, delle specie formate durante l’utilizzo del plasma non termico, solo l’ossigeno atomico potrebbe essere capace di portare a termine questo ambizioso compito. Produrre questo in grandi quantità, potrebbe però causare la formazione di grandi quantità di ozono come risultato di successive reazioni con le molecole di ossigeno, visto che il rapporto fra i suoi reagenti concorrenti O₂ e VOCs è maggiore di 210000:1 (i.e. 21% O₂ comparato con < 1 ppm di VOCs). Questo significa che l’ozono sarebbe inevitabile come prodotto principale. Oltretutto, gli eteroatomi contenuti nei VOCs, come azoto e zolfo, sarebbero rilasciati come ossidi.
Dopo la valutazione di tutti i fattori, è possibile concludere che non è possibile utilizzare i moduli NTP per la pulizia dell’aria in ambienti chiusi senza indugi. Un alto apporto di energia all’interno del sistema provoca concentrazioni inaccettabili di ROS, mentre un basso apporto di energia crea prodotti parzialmente ossidati i quali hanno effetti irritanti in alcuni casi peggiori di quelli provocati dai loro precursori. Allo stesso tempo, il rilascio di ROS, e in particolar modo di ozono, può essere previsto anche in quest’ultimo caso.
La fotocatalisi è il fenomeno naturale in cui una sostanza, detta fotocatalizzatore, attraverso l’azione della luce (naturale o artificiale) modifica la velocità di una reazione chimica. Nella fotocatalisi, in presenza di aria e luce, si attiva un processo ossidativo che porta alla decomposizione delle sostanze organiche e inorganiche che entrano in contatto con la superficie del fotocatalizzatore. Il processo chimico che sta alla sua base è in pratica un’ossidazione che si avvia grazie all’azione combinata della luce e dell’aria. Questi due elementi, a contatto con le superfici, favoriscono l’attivazione della reazione di foto-ossidazione e la conseguente decomposizione delle sostanze organiche e inorganiche, dei microbi, degli ossidi di azoto, dei composti aromatici policondensati etc.
L’ossidazione fotocatalitica (PCO), o fotocatalisi eterogenea, avviene quando un semiconduttore fotocatalizzatore è irradiato da un fotone di luce che trasporta una quantità di energia più elevata della “banda energetica” del fotocatalizzatore. Nella PCO il semiconduttore utilizzato è il diossido di titanio (TiO₂). Il diossido di titanio è un fotocatalizzatore attivabile mediante una radiazione elettromagnetica di opportuna lunghezza d’onda; questo, influendo sulla velocità di una reazione chimica, ne diminuisce l’energia di attivazione, rendendo il processo termodinamicamente più favorito. Dal punto di vista dei materiali, questo materiale può essere considerato un sistema eterogeneo formato da un insieme di particelle in stretto contatto con il mezzo di reazione, gassoso o liquido. Le reazioni di ossidoriduzione e le trasformazioni molecolari foto-indotte avvengono quindi sulla superficie del biossido di titanio, in una serie di processi a catena con trasferimento di elettroni ed energia.
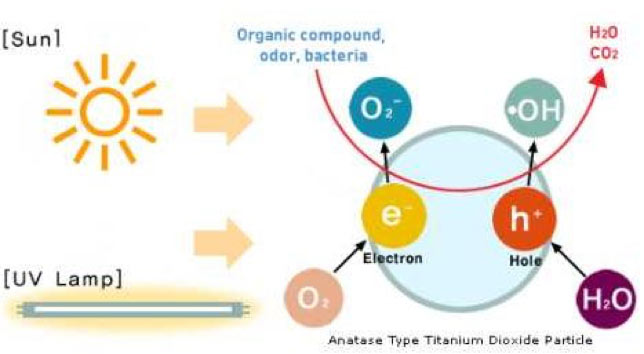
Il biossido di titanio, nella sua forma anatasio, soddisfa tutte le condizioni sebbene solo il 5% della radiazione visibile, la porzione dei raggi UV-A, riesce ad attivarlo. Esso è dunque ampiamente utilizzato nei processi che fanno uso di reazioni fotocatalitiche. La promozione di un elettrone dalla banda di valenza alla banda di conduzione può avvenire per mezzo dell’assorbimento di un fotone, sempre se viene rispettata la condizione: ≤ hν (energia termica minore o uguale al prodotto della costante di Planck e della frequenza di fotoni incidenti), con la formazione di una coppia elettrone-lacuna. Possiamo rappresentare la reazione fotosensibile del TiO₂ nel seguente modo:
![]()
Affinché gli elettroni dello stato di valenza (livello più basso di energia) si eccitino e passino al livello di conduzione (livello energetico più alto), è necessario che i fotoni incidenti abbiano un’energia superiore al band gap EBG, pari a 3,2 eV per l’anatasio. Ricordando che, per la luce, l’energia è legata alla frequenza ν del fotone, che è data dal rapporto tra la velocità della luce c (circa 3· m/s) e la lunghezza d’onda λ, per mezzo della costante di Planck:
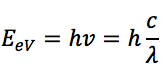
Si ricava che:
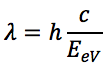
Sapendo quindi che
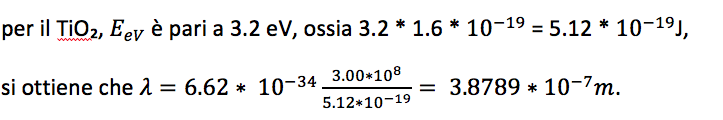
Con questo valore si può affermare che, per l’attivazione del TiO₂, è richiesta una radiazione con lunghezza d’onda inferiore a 388 nm. Una volta generati, in assenza di fenomeni di ricombinazione, la lacuna e l’elettrone possono migrare alla superficie del fotocatalizzatore in vari modi e quindi reagire con le specie adsorbite in superficie.
Per esempio, quando la molecola che entra in contatto superficialmente con il semiconduttore è donatore (D) di elettroni (ad esempio: etanolo, metanolo), questa può reagire con la lacuna fotogenerata presente, ossidandosi a D⁺. Se invece sulla superficie del semiconduttore si deposita una molecola accettore di elettroni (A) (come ossigeno o perossido di idrogeno), allora gli elettroni nella banda di conduzione del fotocatalizzatore possono reagire con tale specie riducendola ad A⁻.
Una caratteristica del TiO₂ è il forte potere ossidante delle lacune fotogenerate h⁺, che possono reagire con l’acqua adsorbita in superficie, con la formazione di un radicale ossidrile altamente reattivo ( · OH). I radicali ossidrili e le lacune fotogenerate riescono ad ossidare la maggior parte dei contaminanti organici: .
![]()
L’ossigeno agisce da accettore di elettroni portando alla formazione dello ione superossido. Anche lo ione super-ossido è fortemente reattivo, risultando in grado di ossidare le molecole organiche:
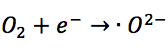
Per quanto riguarda l’influenza della lunghezza d’onda sulla velocità della reazione, conformemente alle considerazioni teoriche precedentemente esposte riguardo all’energia del band gap, si osserva che la velocità tende a zero per λ > 400 nm. Inoltre per essere effettivamente in regime fotocatalico eterogeneo, i reagenti non devono assorbire la radiazione incidente.
Possibili passaggi della PCO:
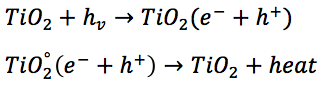
Produzione radicali ossidrili:
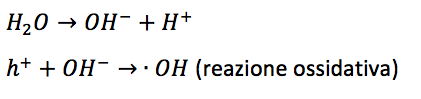
Produzione di superossido:
(reazione di riduzione)
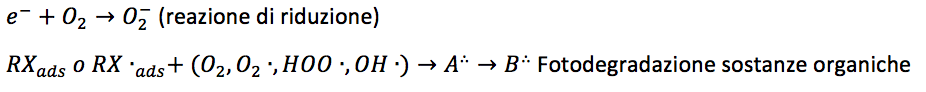
A = intermedi perossidici o ossidrilici
B = prodotti di degradazione o di mineralizzazione (CO₂, H₂O)
In genere la specie che fa da accettore di elettroni è costituita da molecole di ossigeno che sono trasformate in radicali anionici chiamati ioni superossido O°2- e che portano ad un’ulteriore formazione di radicali · OH. Il processo di ossidazione può avvenire direttamente per mezzo delle lacune o mediante i radicali · OH, sia in forma libera che adsorbita. Il percorso di ossidazione porta in molti casi alla completa mineralizzazione delle sostanze organiche per ottenere come prodotti finali CO₂ e H₂O.
La concentrazione dell’ossigeno ha un profondo effetto sulla velocità di decontaminazione nell’ambiente; l’attività fotocatalitica viene quasi completamente soppressa in assenza di ossigeno. La buca nella banda di valenza è capace di ossidare sia le specie organiche adsorbite per formare radicali organici, sia l’acqua o gli ioni ossidrili per formare radicali ossidrili. In genere i substrati organici non vanno incontro ad un diretto trasferimento di h⁺; piuttosto sono i radicali · OH adsorbiti sulla superficie del catalizzatore i responsabili primari della loro distruzione. Oltre a questi radicali è importante la presenza di ossigeno, il cui principale effetto è quello di agire come trappola per gli elettroni e⁻, portando alla generazione di radicali , prevenendo la ricombinazione di h⁺ ed e⁻, fattore principale della lentezza dei processi di degradazione.
I ricercatori hanno stimato che l’efficienza della tecnologia PCO, installata in un edificio adibito a uffici con sistemi HVAC avrebbe dovuto superare il 17% per permettere una riduzione del 50% della ventilazione dell’edificio. Un esperimento del laboratorio di Berkeley ha dimostrato che la conversione della maggior parte dei composti organici ha superato il 19%, confermando la sua efficacia. In numerosi casi, la conversione ha toccato livelli del 75%. Alcuni test hanno rilevato la generazione di formaldeide e acetaldeide dalla parziale ossidazione dei composti organici volatili.
Alcuni studi hanno dimostrato la degradazione dei Microcystin-LR, tra i più comuni e tossici idrosolubili cianotossici emessi dallo sviluppo dei cianobatteri, a seguito della PCO (Triantis et al.). inoltre è stato dimostrato l’efficacia della PCO come tecnica per creare rotture localizzate nel doppio filamento del DNA (rottura dei legami idrogeno tra purine e pirimidine), ciò a dimostrare che la tecnologia in questione ha un ruolo nella distruzione delle particelle virali (Suzuk et al.).
La PCO ha rivelato inoltre il possesso di un controllo positivo sui batteri Bacillus e sulla riduzione dei microbi presenti nell’aria delle sale operatorie e di altre ambientazioni cliniche (Cram et al.).
Glenn Morrison et al. Hanno testato 3 dispositivi fotocatalitici i quali hanno mostrato emissioni di ozono relativamente basse. La quantità di ozono prodotta dipende principalmente dalla tipologia di lampada UV utilizzata: nella PCO si possono usare diversi tipi di lampade UV, incluse le black lights (UV-A: ampia lunghezza d’onda; da 400 a 315 nm), le lampade germicida (UV-C: breve lunghezza d’onda; da 280 a 200 nm), e le lampade che generano ozono (vacuum UV [UV-V]; lunghezza d’onda minore di 200 nm).
Quasi tutti i contaminanti organici dell’aria, gassosi e microbi sono soggetti alla decomposizione da parte della PCO. L’efficacia dell’ossidazione dipende principalmente dai gruppi funzionali dei contaminanti che passano attraverso il dispositivo. Efficacia maggiore è stata osservata per composti ossigenati come alcoli, chetoni e alcune aldeidi; efficacia intermedia per i composti aromatici; e bassa efficacia per i clorocarboni. I vantaggi della PCO sono la relativamente bassa caduta di pressione, l’abilità a trattare un’ampia varietà di composti, e un teoricamente lungo ciclo di vita del processo di reazione. Gli svantaggi includono l’energia della lampada, i costi di sostituzione della lampada e la probabilità di generazione di ozono dipendente dalla tipologia di lampada utilizzata (e.g. lampada UV-V 185 nm produce ozono). In uno studio del 1992 condotto da Ohtani et al., però, è stato dimostrato che le radiazioni UV di lunghezza d’onda compresa tra 200 nm e 400 nm, in particolare gli UV-C (254 nm) a contatto con diossido di titanio (TiO₂) causano reazioni chimiche che provocano la decomposizione delle molecole di ozono. Inoltre, durante le reazioni caratteristiche della PCO, c’è la possibilità di processi di ossidazione incompleti, i quali producono sotto-prodotti di reazione che possono essere maggiormente tossici o dannosi dei composti originali.
Un altro svantaggio della tecnologia PCO è che i catalizzatori possono essere contaminati (avvelenati) da reagenti aerodispersi e/o da prodotti di ossidazione, con il risultato di una riduzione dell’efficienza o un totale fallimento del processo. La decomposizione incompleta di alcuni contaminanti organici e una netta produzione di formaldeide, acetaldeide, acido formico e acido acetico sono stati mostrati da Hogson et al. In uno studio del 2007.
Il processo di ossidazione fotocatalitica è influenzato da numerosi parametri, i principali sono:
Sicuramente il grado di umidità gioca un ruolo fondamentale. E’ stato provato che tracce di vapore d’acqua sono essenziali per mantenere l’attività fotocatalitica per lunghi periodi, quantità elevate inibiscono tuttavia il processo: in primo luogo, l’acqua compete con le sostanze organiche presenti per l’occupamento dei siti attivi sul TiO₂ e questo avviene a seguito della formazione di legami a idrogeno con i gruppi ossidrilici presenti sulla superficie del catalizzatore, inoltre la presenza di acqua diminuisce notevolmente la degradazione di specie idrofiliche (ad esempio la formaldeide, l’acetone e il metanolo). Per molti composti, invece, un aumento dell’umidità favorisce la conversione ossidativa poiché il vapore d’acqua può inibire la formazione di depositi di carbonio sulla superficie del TiO₂ a causa del comportamento superidrofilico del film.
Per quanto riguarda la concentrazione delle sostanze inquinanti, è stato osservato che il grado di conversione aumenta esponenzialmente all’aumentare della concentrazione iniziale d’inquinante fino ad un certo valore variabile a seconda della specie chimica considerata, oltre il quale rimane costante.
Il flusso del gas è uno dei parametri più importanti che influenzano il processo d’ossidazione. Questo influenza il trasferimento di massa e il trasporto degli inquinanti alla superficie del catalizzatore. Aumentando il flusso si favorisce la turbolenza all’interno del reattore e si aumenta il trasferimento di massa in fase gas, portando quindi più inquinanti sulla superficie del TiO₂. Tuttavia, un flusso troppo elevato può essere causa della saturazione dei siti attivi, per cui lo stato di equilibrio fotocinetico non viene raggiunto con la conseguente diminuzione (esponenziale) del fattore di conversione.
L’intensità della fonte d’irradiazione influenza l’ordine della reazione di fotocatalisi. Per l’illuminazione superiore 1000-2000 µW/, la velocità di degradazione cresce con il quadrato del flusso di fotoni, per valori inferiori l’aumento è lineare. Anche la lunghezza d’onda della radiazione gioca un ruolo importante nella fotocatalisi. Si osserva per esempio che una lampada con λ=254 nm dà risultati migliori in termini di velocità e rendimento del processo fotocatalitico rispetto ad una con λ=365 nm.
Per aumentare l’efficienza fotocatalitica del biossido di titanio è necessario produrlo per almeno l’80% nella fase cristallina dell’anatasio e possibilmente sotto forma di nano particelle di dimensioni comprese tra qualche decina e poche centinaia di micron così da aumentare la densità di particelle attivabili nella stessa superficie.
Le diverse attività di ricerca portate avanti nel tempo hanno evidenziato come, passando a dimensioni inferiori ai 100 nanometri, le proprietà di diversi elementi cambino sensibilmente sotto il profilo fisico e chimico, sia per la diversa configurazione delle particelle e sia per l’incremento significativo del rapporto superficie/volume e superficie/peso. Una data massa di particelle di dimensioni micrometriche ha una superficie esterna migliaia di volte inferiore ad una massa uguale ma di particelle di dimensioni nanometriche. Nelle diverse attività di ricerca e caratterizzazione dei materiali impiegati nelle sintesi di nanoparticelle, si sono evidenziati interessanti fenomeni correlati al TiO₂ nonché ai coatings di TiO₂ anche drogato con altri elementi. Il biossido di titanio infatti ha mostrato spiccate proprietà fotocatalitiche ovvero, applicato sotto forma nanoparticellare su superfici di sperimentazione, una volta colpito da radiazioni UV/LED, ovvero da radiazioni di lunghezza d’onda λ < 400 nm e di energia almeno pari ad hv> 3,2 eV si carica facendo passare un elettrone in banda di valenza. Questo fenomeno dà di fatto luogo alla seguente reazione:

Generando pertanto dei gruppi ossidanti molto forti. Questi effetti, incrementati significativamente dalle dimensioni nanoparticellari del TiO₂, conferiscono alle superfici sperimentali trattate proprietà ossidanti se colpite dalla luce solare o UV, in grado di manifestare effetti antibatterici e di abbattere diversi elementi contaminanti dagli NOX fino ad elementi biologici e chimici impiegati anche come armi chimiche e batteriologiche. Per sfruttare queste proprietà nel trattamento dell’aria, sono stati depositati i principi attivi nanoparticellari su degli honeycombs, piastrelle ceramiche porose caratterizzati da setti di attraversamento di forma conica di dimensioni variabili. Colorobbia ha inoltre usato come metodo di irraggiamento degli honeycombs dei LED al posto di lampade UV.
Dispositivo che sfrutta le proprietà ottiche di alcuni materiali semiconduttori per produrre fotoni a partire dalla ricombinazione di coppie elettrone-lacuna. Il colore della radiazione emessa è definito dalla distanza in energia tra i livelli energetici di elettroni e lacune e corrisponde tipicamente al valore della banda proibita del semiconduttore in questione. Dispositivi basati su LED near-UV sono da tempo disponibili sul mercato; un comune utilizzo è la sostituzione delle lampade a luce nera (o lampade di Wood, Hg a bassa pressione) nei dispositivi destinati ad identificare la presenza di particolari vernici fluorescenti agli UV come misura anticontraffazione di documenti e banconote. Lunghezze d’onda più corte sono raggiungibili con diodi più costosi, ma comunque commercialmente disponibili per λ fino a 247 nm. Poiché la sensibilità agli UV dei microorganismi dipende approssimativamente dallo spettro di assorbimento del DNA (con un picco a circa 260 nm, per il quale si ha rottura della catena), i LED emettenti radiazioni UV a 250 – 270 nm sono ritenuti ottimi candidati per la realizzazione di dispositivi per la disinfezione e la sterilizzazione. Recenti studi hanno mostrato che anche i LED UV-A (365 nm), già disponibili sul mercato hanno un’efficace attività batteriostatica e battericida.
Alcuni brevetti descrivono il metodo di azione fotocatalitica secondo cui la generazione di radicali ossidrili ha azione microbicida; altri brevetti descrivono invece sistemi di filtrazione per ambienti civili nei quali l’utilizzo di dispositivi fotocatalitici permette di superare i problemi legati ai fenomeni di ostruzione che si hanno nei comuni filtri per la depurazione dell’aria.
Il supporto è stato preparato mediante immersione in una sospensione nanoparticellare al 6% in diossido di titanio a pH acido. Il supporto così ottenuto è stato sottoposto al seguente ciclo termico in forno discontinuo: rampa termica di 10 ore fino a 700 °C, plateau a 700 °C per 1 ora. La quantità di nanoparticelle depositate è stata valutata in 100 g/ espressi come TiO₂.
Sono stati impostati intervalli di campionamento di 15 minuti, della durata di 5 minuti l’uno, per un totale di 6 misure.
Ottima efficienza nella decomposizione degli ossidi di azoto da parte dell'honeycomb. Per questa ragione il materiale può essere un buon candidato per costituire la parte attiva di filtri per la decontaminazione ambientale degli inquinanti gassosi e di sostanze tossiche volatili.
| Tempo (min) | ΔNO% | ΔNOx% |
|
5 |
0.0 |
0.0 |
|
25 |
64.5 |
50.2 |
|
45 |
73.8 |
59.8 |
|
65 |
82.2 |
71.2 |
|
85 |
86.0 |
79.9 |
|
105 |
89.0 |
88.6 |
Abbattimento percentuale normalizzato di NO e NOx
Lo sviluppo della specie intermedia NO₂ segue un andamento a campana indice della completa trasformazione degli NO in NO₂ e della loro ulteriore ossidazione secondo lo schema di reazione:
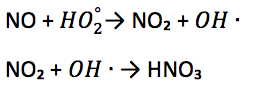
Questo andamento è indice della elevata efficienza fotocatalitica del sistema.
Un aspetto peculiare del TiO₂, simultaneo al fenomeno fotocatalitico, è rappresentato dall’idrofilia fotoindotta (PIH). In pratica, dopo illuminazione, parte degli elettroni e lacune fotogenerati reagiscono in maniera differente, ossia, gli elettroni tendono a ridurre i cationi in e le lacune ossidano gli anioni . Mediante questo processo, gli atomi di ossigeno sono espulsi e le vacanze che così si formano vengono ad essere occupate da molecole d’acqua. I gruppi ossidrilici, che si legano alle molecole di acqua con legami a idrogeno, rendono idrofila la superficie di TiO₂. L’aumento del tempo di esposizione alla luce della superficie di TiO₂, riduce l’angolo di contatto con l’acqua. L’acqua, anziché raccogliersi in gocce, tende così a formare sulla superficie un film continuo. Ovviamente, secondo la composizione ed il trattamento, una superficie può presentare un’attività più spiccatamente fotocatalitica e meno idrofila, o viceversa.
In fase gassosa, la reazione di decomposizione dei contaminanti organici, quali NOx o VOCs, è influenzata dalla disponibilità di O₂ o dall’umidità presente nel sistema, ma anche dal tipo di inquinante da mineralizzare. Uno dei maggiori problemi, in fase gas, è la deattivazione del fotocatalizzatore, a causa dell’adsorbimento di prodotti intermedi di reazione sulla sua superficie.
I principali composti inquinanti sono:
Esempio di degradazione degli NOx con fotocatalisi
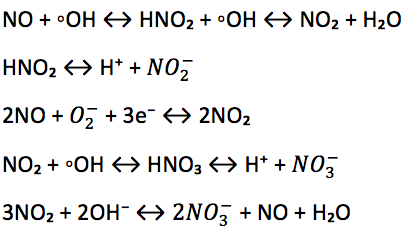
Il processo fotocatalitico genera i radicali ossidrilici e gli ioni superossido che interagiscono con NO e NO₂ presenti nell’aria degradandoli a sali nitrati (assolutamente innocui) e acqua. Tra i sottoprodotti delle reazioni chimiche della fotocatalisi ne citiamo alcuni:
La degradazione del biossido di azoto forma essenzialmente nitrati solubili in acqua e, eventualmente nitriti. La quantità formata di queste specie è molto contenuta per cui esse non costituiscono problema per le acque dilavate. Nel caso di manufatti non esposti, le molecole di nitrato di calcio, risultanti dalla reazione di fotossidazione, rimangono nella superficie fotocatalitica come sostanze inerti.
La formaldeide viene degrada a monossido di carbonio oppure a biossido di carbonio. A causa della concentrazione relativamente bassa di formaldeide, anche le concentrazioni dei prodotti formati saranno molto basse ed inferiori di circa 100 volte a quelle normalmente presenti nell’ambente. L’eventuale ossidazione di formaldeide porterebbe alla formazione di biossido di carbonio ed a tracce di acido formico che sarebbero comunque assorbite dal substrato alcalino della superficie fotocatalitica.
Il biossido di zolfo viene ossidato ad acido solforico, a sua volta immediatamente adsorbito dal substrato alcalino della superficie fotocatalitica. Il risultato è la formazione di solfato di calcio, debolmente solubile in acqua. Il solfato di calcio, comunemente conosciuto come gesso, non costituisce problema per l’ambiente.
L’ossidazione del monossido di carbonio porta alla formazione di biossido di carbonio, sostanza praticamente inerte. Il monossido di carbonio potrebbe anche essere ossidato dai radicali OH portando alla formazione di radicali idrogeno (H). Tali radicali reagiscono velocemente con l’ossigeno dell’aria formando radicali idroperossido: H + O₂ ⇒ HO₂ Quest’ultimo radicale possiede proprietà ossidanti molto più spiccate del radicale OH, per cui il monossido di carbonio potrebbe amplificare le proprietà ossidanti della superficie fotocatalitica con evidente aumento della sua capacità depurativa.
La degradazione di benzene su superfici fotocatalitiche procede a velocità molto basse stante la scarsa reattività del benzene verso il radicale OH. Le molecole ossidate possono comunque trasformarsi in composti più semplici quali aldeidi o acidi bivalenti che non portano a nessun effetto ambientale. In alternativa, si può ipotizzare che il benzene possa addizionare radicali OH e trasformarsi quindi in fenolo, sostanza questa solubile in acqua e comunque di scarso interesse ambientale a causa delle basse concentrazioni risultanti.
L’evoluzione del particolato sulle superfici fotocatalitiche è ancora oggetto di speculazione scientifica. Con ogni probabilità le particelle che costituiscono il particolato atmosferico vengono attratte sulla superficie a causa della presenza di cariche libere. Una volta sulla superficie, le particelle potrebbero reagire con i radicali liberi o con molecole di acqua e di ossigeno, degradandosi a sostanze organiche ossigenate solubili in acqua. La parte inorganica, costituita da composti già ampiamente ossidati, non dovrebbe invece alterarsi. Possiamo quindi dedurre che i residui della fotocatalisi possono essere ritenuti assolutamente trascurabili.
L’effetto battericida e virucida per azione fotocatalitica del TiO₂ è dovuto alla formazione di ROS tra cui il radicale ossidrile · OH , generate dal sistema sinergico diossido di titanio-luce. La maggior parte degli studi ha condotto sempre alla stessa conclusione, ovvero che il radicale ossidrile è la specie principale coinvolta nell’azione battericida e virucida della fotocatalisi.
I radicali ossidrili, avendo una durata estremamente breve, devono essere generati in prossimità della membrana affinchè siano in grado di eliminarne i componenti. Il tempo di vita breve ed il fatto di essere prodotti su una superficie limitata li rendono innocui verso le persone.
I più potenti sistemi di ossidazione avanzata si basano sulla generazione di radicali ossidrili. Il radicale ossidrile è un agente ossidante estremamente potente. Proprio per la sua forte capacità ossidativa, l’ossidazione fotocatalitica può effettivamente igienizzare, deodorare e purificare l’aria, l’acqua e diverse superfici.
La fotocatalisi non solo uccide le cellule dei batteri, ma le decompone. È stato verificato che il biossido di titanio è più efficace di qualsiasi altro agente antibatterico, perché la reazione fotocatalitica avviene anche quando ci sono cellule che coprono la superficie e la moltiplicazione dei batteri è attiva, attivandosi sulla superficie ed aggirando il biofilm creato dai batteri è efficace dove i sanificanti chimici tradizionali risultano meno performanti. Inoltre, l'endotossina derivante dalla morte della cellula viene decomposta per merito dell'azione fotocatalitica. Il biossido di titanio non si degrada e mostra un effetto antibatterico e virucida a lungo termine. In linea generale, la disinfezione mediante biossido di titanio è 3 volte più efficace di quella che si ottiene con il cloro, e 1.5 volte dell’ozono.
Tutti i costituenti cellulari, come polisaccaridi, lipidi, proteine e acidi nucleici possono essere attaccate dai ROS formati durante la fotocatalisi. Tuttavia la membrana cellulare è il bersaglio iniziale dell’attacco fotocatalitico. Considerando come esempio i batteri Gram-negativi, l’ossidazione dei componenti della membrana esterna da parte dei ROS provoca un incremento della permeabilità della cellula. Conseguentemente, i ROS possono facilmente raggiungere la membrana citoplasmatica, dove avviene anche la perossidazione della membrana lipidica. Il conseguente disordine strutturale e funzionale della membrana citoplasmatica permette ai ROS l’ingresso nella cellula, dove essi interferiscono negativamente con la replicazione del DNA e con l’attività respiratoria, dovuta alla diretta ossidazione del coenzima A nella sua forma dimerica. In definitiva, l’attacco dei ROS provoca la perdita della vitalità della cellula e la morte cellulare. Le evidenze indicano che la reazione fotocatalitica con TiO₂ risulta in una continua azione battericida, anche dopo il termine dell’illuminazione UV.
La fotocatalisi UV-TiO₂ sembra essere efficace nell’inattivazione di tutti i tipi di microrganismi, dipendentemente però dal tipo di microrganismo e dal tempo di contatto. Le performance di disinfezione del TiO₂ modificato sotto luce visibile rimangono comunque peggiori di quelle sotto irradiazione UV, anche se alcune ricerche affermano che se le molecole organiche sono spinte attraverso un modulo con tecnologia fotocatalitica troppo velocemente possono verificarsi reazioni incomplete e dal sistema possono uscire acetaldeide e formaldeide.
Alcuni studi hanno inoltre dimostrato come i fenomeni di stress ossidativo cellulare e conseguenti danni cellulari, alterazioni della risposta immunitaria, genotossicità e infiammazione siano spesso causati da un'elevata concentrazione di nanoparticelle di TiO₂ sia esposte a irradiazione UV che non. Ad esempio, è stato sperimentato come il TiO₂ anatasio nanoparticellare possa indurre un danno ossidativo nelle cellule epiteliali bronchiali umane. Inoltre il biossido di titanio induce la formazione di specie radicaliche centrate sull'ossigeno (ROS), i radicali liberi, che rappresentano degli importanti modulatori dei processi di segnalazione cellulare: ne consegue che l'esposizione delle cellule a nanoparticelle di TiO₂ può, tramite un'elevata formazione di ROS, influire sulla segnalazione cellulare che controlla i processi come la proliferazione cellulare, l'infiammazione e la morte cellulare.
In commercio esistono principalmente tre tipi di lampade UV: A, B e C, ognuna rappresentante una differente sezione dello spettro UV. Il tipo C, conosciuto come UV-C, è la forma utilizzata per l’attività germicida. Quando la reazione UV-C è utilizzata per propositi germicidi, ci si riferisce ad essa come UVGI, irradiazione ultravioletta germicida.
L’UVGI “disattiva” o uccide i microrganismi, inclusi virus, batteri, muffe e altri funghi distruggendo il loro DNA. “Disattivare” significa che il loro organismo non viene necessariamente ucciso ma non può più riprodursi. Alcuni organismi vengono disattivati dopo microsecondi di esposizione mentre altri richiedono un tempo di esposizione più lungo. Tuttavia, l’efficacia degli UVGI dipende da un grande numero di fattori, inclusi:
Inoltre la radiazione UV-C reagisce con l’ossigeno e il vapore acqueo nell’aria a generare concentrazioni di radicali ossidrili nel range da 0.1 ppt a 1 ppb. I radicali ossidrili possono reagire con i lipidi e le proteine nella membrana cellulare dei microrganismi (inclusi batteri e virus) all’interno della camera di radiazione uccidendoli, contribuendo così al processo di sanificazione. Entrambi i meccanismi possono accadere in concomitanza.
Il sistema non è un filtro, esso disattiva le particelle rimaste nel flusso d’aria, le quali nel caso di spore fungine per esempio, possono causare una risposta umana negativa alle micotossine.
Il range di lunghezza d’onda più efficace per la disattivazione dei microrganismi è compreso tra 220 e 300 nm, con picchi di efficacia attorno ai 265 nm.
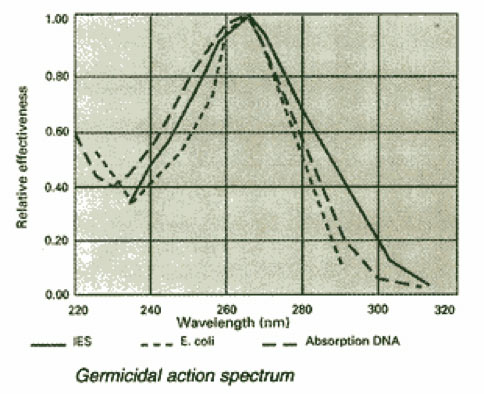
La fonte tipica di UV-C per sistemi di disinfezione di acqua e aria industriali e residenziali sono le lampade a vapori di mercurio a bassa pressione, le quali emettono principalmente la lunghezza d’onda quasi ottimale di 253.7 nm. L’efficacia dei sistemi a UV-C di disattivare i microrganismi nell’aria e/o sulle superfici è stata ampiamente dimostrata. L’esperienza suggerisce che l’uso di un flusso d’aria in movimento non fornisce tassi di uccisione favorevoli a causa del breve periodo di contatto. In condizioni ideali, tassi di disattivazione e/o uccisione del 90% o più alti possono essere raggiunti ma dipende dai seguenti fattori: il tipo di contaminante microbico, le caratteristiche delle specie, fattori fisici o meccanici come l’intensità dell’UV-C, il tempo di esposizione/contatto, la distanza e il posizionamento della lampada, il ciclo di vita della lampada e la sua pulizia, il flusso dell’aria, la temperatura, l’umidità relativa e la miscelazione dell’aria.
Tuttavia, ci sono prove limitate riguardo gli effetti diretti delle radiazioni UV-C sulla salute.
La Columbia Analytical Services ha testato i dispositivi che utilizzano questa tecnologia con l’intento di misurare i tipi e le concentrazioni dei sottoprodotti organici dell’ossidazione e la quantità di ozono prodotti durante il funzionamento, in breve, i dati raccolti hanno indicato che:
È stato dimostrato che il trattamento UV è meno efficace del trattamento TiO₂-UV. L’uso di un fotocatalizzatore in molti casi diminuisce il bisogno di alte intensità di radiazioni e promuove la diminuzione del tempo di contatto necessario.
Ibanez e collaboratori hanno verificato che non è possibile disattivare i batteri Enterobacter cloacae, E. coli, P. aeruginosa e Salmonella tiphimurium con un’irradiazione UV di 55 W/. Tuttavia associando l’irradiazione UV di 55 W/ con 0.1 g/L di TiO₂ è stata ottenuta una riduzione logaritmica dei valori per tutti i test effettuati mantenendo lo stesso tempo di contatto.
L’ozono è una molecola costituita da tre atomi di ossigeno. È molto meno stabile della più comune molecola di ossigeno. A livelli elevati, a volte a livelli che si possono trovare nell’aria sia interna che esterna, l’ozono è un potenziale pericolo per la salute. Inoltre, l’ozono può reagire con pitture o altri composti chimici usati per le costruzioni edili a formare sottoprodotti che possono causare preoccupazioni per la salute. L’ozono è formato dall’azione delle radiazioni con a lunghezza d’onda e diossido di azoto. In presenza di VOCs, l’equilibrio favorisce la formazione di elevati livelli di ozono. La concentrazione media di ozono nell’aria esterna varia nel corso della giornata, a seconda della fascia oraria di misurazione, tra 0.02 e 0.08 ppm.
La tossicità dell’ozono dipende dalla concentrazione, dalla durata del tempo di esposizione e dalla tipologia di attività effettuata durante l’esposizione. Effetti acuti in breve tempo includono sintomi respiratori, cambiamenti nelle funzioni polmonari, aumento della reattività delle vie aeree e infiammazione di queste.
Effetti sulla salute associati alle concentrazioni di ozono misurate:
|
Effetti sulla salute |
Concentrazione media 1 ora |
Concentrazione media 8 ore |
|
Leggeri sintomi respiratori |
0.13 – 0.25 ppm |
0.06 – 0.12 ppm |
|
Reazioni infiammatorie |
0.20 – 0.41 ppm |
0.09 – 0.16 ppm |
|
Aumento dei sintomi in asmatici |
0.10 – 0.40 ppm |
0.05 – 0.15 ppm |
Visti i gravi effetti sulla salute dovuti all’esposizione all’ozono, molti paesi e alcune organizzazioni hanno trovato necessario introdurre norme per limitare l’esposizione a questo composto.
|
Ente |
Italia (Ministero della Salute) |
Olanda |
Canada |
Who |
Ashrae |
EPA |
FDA |
OSHA |
NIOSH |
OMS |
|
Lim. O₃ |
Lavoro leggero = 0,10 ppm |
150-200 μg/m^3 per 1h |
240 μg/m^3 per 1h |
150-200 μg/m^3 per 1h |
235 μg/m^3 per 1h |
235 μg/m^3 per 1h |
0,1 ppm da |
|||
|
Lavoro moderato = 0,08 ppm |
100-120 μg/m^3 per 8h |
40 μg/m^3 per 8h |
100-120 μg/m^3 per 8h |
100 μg/m^3 per 8h |
non superare |
100 μg/m^3 per 8h |
||||
|
Lavoro pesante = 0,05 ppm |
mai |
|||||||||
|
ppm per 8h |
Limite proposto = 0,06 ppm per 8h |
0,05-0,06 ppm per 8h |
0,02 ppm per 8h |
0,06 ppm per 8h |
0,05 ppm per 8h |
0,08 ppm per 8h |
0,05 ppm per 8h |
0,1 ppm per 8h |
0,1 ppm |
0,05 ppm per 8h |
Inoltre sono state introdotte normative riguardanti le concentrazioni limite di altri composti presenti nell’aria e potenzialmente pericolosi per la salute dell’uomo. Di seguito ne riportiamo alcuni:
|
Inquinante (udm) |
Olanda |
Canada |
Norvegia |
WHO Europa |
ASHRAE |
EPA |
|
CO₂ (mg/m3) |
- |
6300 |
1800 |
- |
1800 |
- |
|
CO (mg/m3) |
10 (8 h) 40 (1 h) |
13 (8 h) 29 (1 h) |
10 (8 h) 25 (1 h) |
10 (8 h) 30 (1 h) 60 (30 min) 100 (15 min) |
10 (8 h) 40 (1 h) |
10 (8 h) 40 (1 h) |
|
NO₂ (μg/m3) |
300 (1 h) 150 (24 h) |
480 (1 h) 100 (long term) |
200 (1 h) 100 (24 h) |
400 (1 h) 150 (24 h) |
100 (anno) |
100 (anno) |
|
Formaldeide (μg/m3) |
120 (30 min) |
120 (livello di azione) |
60 |
100 (30 min) |
100 (30 min) |
- |
|
Particolato (μg/m3) TSP |
40 (anno) 140 (24 h) - - - - |
- - 40 (long term) 100 (1 h) - |
40 (anno) - - - 90 (8 h) |
- - - - 120 (24 h) |
50 (anno) 150 (24 h) - - - |
50 (anno) 150 (24 h) - - - |
|
VOC totali (μg/m3) |
- |
- |
400 |
- |
- |
- |
|
Radon (Bq/m3) |
200 |
800 |
200 |
200 (nuove abitazioni) 400 (vecchie abitazioni) |
150 |
150 |
|
SO₂ (μg/m3) |
350 (1 h) |
50 (long term) 1000 (5 min) |
- |
350 (1 h) 500 (10 min) |
80 (anno) 365 (24 h) |
80 (anno) 365 (24 h) |